中国国家薬品監督管理局(NMPA)への登録代行その他
- 中国NMPAへの医療機器、保健食品、機器の登録代行
1. 中国NMPA認証とは
- 中国市場にて医療機器、医薬品、医薬品包材、保健食品を販売するための要件。
- 日本国に於ける厚生労働省所管の製造販売承認書に相当する認証。
(米国のFDAによるPMA認証、欧州のCE認証に準ずる)
中国NMPA登録と届出について
- NMPA認証を申請する製品の分類等により、「登録」となるか「届出」かが異なる
対象区分:
医療機器の場合:第一類(届出)、第二類、第三類(登録)
保健食品の場合:栄養補充剤特定ビタミン・ミネラル22種類)(届出)、27機能性保健食品(登録)
- 再登録制:登録証には有効期限の設定あり
(品目によって4年または5年。 登録の維持・継続には有効期限までに登録更新が必要。)
登録の維持・継続には有効期限までに登録更新が必要 - その他:医療機器の変更申請等は別途ご相談ください。
- 再登録制:登録証には有効期限の設定あり
- 中国NMPAへの登録申請製品についての要件
申請者または製造所が在する国家または地域で上市した製品 - 中国NMPAへの登録申請者についての要件
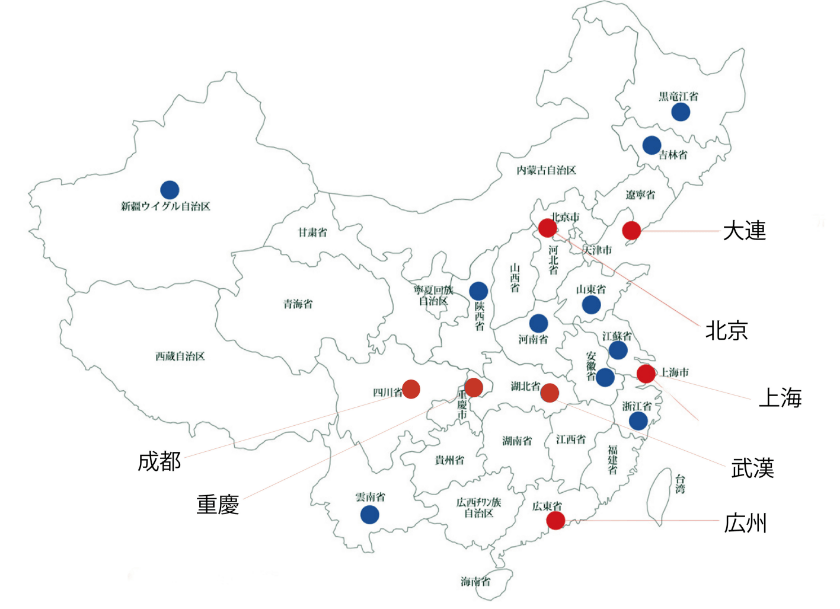
原産国または製造所が在する国家または地域で当該品の販売許可を有する者 - 登録申請時に必要な関連機関・施設の要件
申請者が中国現地に関係先を有しない場合に、予め設定しておくべきもの- 委託する中国国内の代理機構(中国指定代理人)
- 販売サービス機構
2. 登録に要する費用
- 具体的な製品概要をお聞きした上で、以下のとおり各項目別に正式な見積もりをご提示します。
- 登録代行料(製品サンプルの検測試験、翻訳費用、公証費用を除く 一切の費用を含む)
- 製品検測試験費用(参考提示のみ)
- NMPAに支払う申請料(暫定的に医療機器、薬品の申請時に必要とする)
<注>
A.については 対NMPA交渉、試験状況管理、各種調整等、申請着手から登録完了までの途中に発生しうる一切の事柄に追加ありません。 (当初ご予算内で)
B. “製品検測試験料”は、NMPA認定試験機関発行による請求書を添えて、後日実費ご請求を原則とします。 但し、試験前の概算金額デポジット支払いとなる場合有り。 当初の段階では概算を参考見積もりします。 (全体のご予算掌握の為) -
簡単な製品説明によっても概算ご提示できますので、お気軽に電話またはメールにてご相談ください。
お電話:03-3248-1006
メール: - 申請者の製品情報に関して「秘密保持契約」締結の下に、その取扱いには弊社中国法人(大連本部、北京事務所)とも留意いたします。
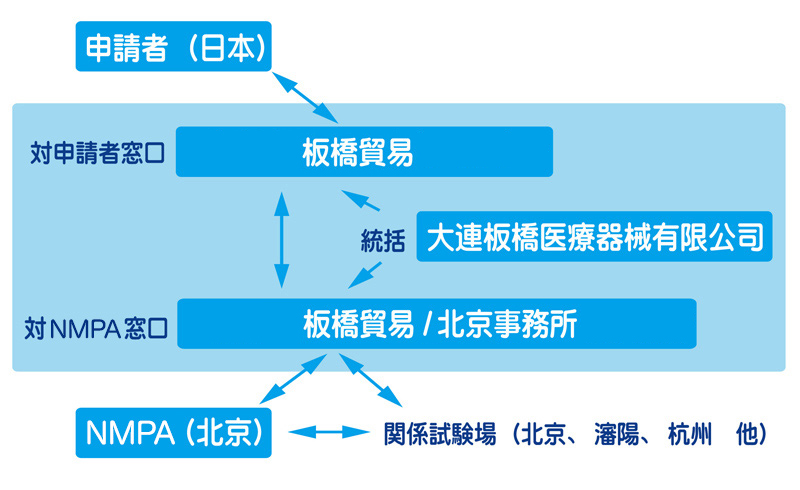
3. 弊社の取組体制
- 弊社グループは日本側と中国側(大連、北京)と2つの側面からキメ細かなサービスとフォローの体制を整え、関係先との密なる意志疎通を図り、早期登録の実現に努めます。
- 日本側:日本語によるコミュニケーション(誤解、曲解を排除)
- 中国側:NMPAとの密なる現場接触